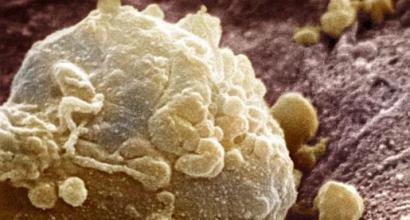
Основной белок миелина. Диета для профилактики демиелинизации
ЭКСПЕРИМЕНТАЛЬНЫЕ СТАТЬИ
Анализ фрагментации основного белка миелина под действием протеасомы
А. В. Бачева1#, А. А. Белогуров2, Н. А. Пономаренко2, В. Д. Кнорре2, В. М. Говорун2,
М. В. Серебрякова3, А. Г. Габибов1,2
1 Химический факультет Московского Государственного Университета имени М. В. Ломоносова, Москва
2 Институт биоорганической химии им. академиков М. М. Шемякина и Ю. А. Овчинникова РАН, Москва
3 Протеомный центр РАМН, НИИ Физико-химической медицины Росздрава РФ # e-mail: [email protected]
РЕФЕРАТ Протеасома - это высокомолекулярный белковый комплекс, служащий для направленной деградации белков в эукариотических клетках. Одной из функций протеасом является генерация пептидов, которые затем экспонируются на клеточной мембране с помощью молекул комплексов гистосовместимости как первого, так и второго класса. Есть все основания полагать, что протеасома принимает непосредственное участие в процессе специфической деградации основного белка миелина (ОБМ), составляющего около 30 % всех белков миелиновой оболочки аксонов нейронов. Детали этого механизма остаются невыясненными. В представленной работе изучены особенности специфической деградации ОБМ протеасомой.
Нами было продемонстрировано, что основной белок миелина (не подвергавшийся убиквитинилированию) является хорошим субстратом как для 20S, так и для 26S протеасомы. Впервые были определены сайты протеолиза ОБМ протеасомой из мозга мышей линий Ва1Ь/С и SJL и показаны значительные различия в паттерне деградации данного нейроантигена, что может свидетельствовать о лучшей презентации фрагментов основного белка миелина на комплексах гистосовместимости в случае мышей, предрасположенных к развитию экспериментального аутоиммунного энцефаломиелита.
ВВЕДЕНИЕ
Рассеянный склероз (РС) - хроническое нейродегенера-тивное заболевание аутоиммунной природы - представляет собой острую медико-социальную проблему, поскольку, как правило, поражает лиц молодого и среднего возраста. Проблема лечения РС остается далекой от разрешения, на сегодняшний день существуют лекарственные препараты, способные в некоторой степени замедлить течение РС, но не излечивать от этой патологии. Деградация нервных волокон, происходящая при рассеянном склерозе, протекает вследствие разрушения миелиновой оболочки нейронов. Одной из биохимических характеристик, которая отличает миелин от других биологических мембран, является высокое соотношение липид/белок. Белки составляют от 25 до 30 % массы сухого вещества миелиновой оболочки. Около 30 % всех белков миелина составляют три изоформы т. н. основного белка миелина (ОБМ). ОБМ является одним из основных аутоантигенов при РС. Ранее нами и другими исследователями было показано, что в деградации ОБМ могут принимать участие каталитические антитела , а также некоторые проте-
азы . Известно, что в любой эукариотической клетке существует специализированная органелла для направленной деградации белков - протеасома, представляющая собой высокомолекулярный белковый комплекс. Одной из функций протеасом является генерация пептидов, которые затем экспонируются на клеточной мембране с помощью молекул комплексов гистосовместимости (МНС) как первого, так и второго класса . Есть все основания полагать, что протеасома принимает непосредственное участие в процессе специфической деградации ОБМ. Детали этого механизма остаются невыясненными. В представленной работе нами были изучены особенности специфической деградации ОБМ протеасомой.
Известно, что 20S протеасома (мультикаталический протеиназный комплекс) - это олигомерная высокомолекулярная (700 кДа) протеиназа, которая может быть выделена индивидуально. Данный комплекс также является каталитическим ядром 26S протеасомы, в составе которой присутствуют одна или две регуляторных 19S субъединицы. Было показано, что и 20S и 26S протеасомы способны деградировать ОБМ . Вопрос о сайт-специфичности
BpeWR. МИНУТЫ
Рис. 1. Зависимость степени гидролиза ОБМ протеасомой от времени. Обозначения: о - 20S протеасома, - 26S протеасома, выделенные из печени аутбредных мышей
деградации ОБМ протеасомой оставался открытым. Кроме того, известно, что при многих воспалительных патологических процессах протеазный комплекс (конститутивная протеасома) переходит в форму иммунопротеасомы, обладающей альтернативной специфичностью и каталитической эффективностью по отношению к процессингу внутриклеточных белков. Скорее всего, это «переключение» имеет непосредственное отношению к различной презентации антигенов в норме и патологии. Паттерн деградации ОБМ иммунопротеасомой до настоящего времени изучен не был.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Протеасома была выделена и очищена по методу, описанному в . Сначала была исследована деградация ОБМ (изоформа с молекулярной массой 18.5 кДа из мозга быка) полным 26S комплексом и каталитической 20S субъединицей, выделенными из печени аутбредных мышей. Как показано на рис. 1, инкубация ОБМ как с 20S, так и с 26S протеасомой приводила к постепенной деградации ОБМ. Уже через 45 мин 20S протеасома полностью гидролизовала основной белок миелина, в то время как 26S протеасо-ме на это требовалось 85 мин. Такое различие в скоростях можно отнести к разному количеству протеасомы: в случае 20S протеасомы соотношение фермент/субстрат составило 2.7/1 (по белку, мкг/мкг) или 1/14.5 (моль/моль), а в случае 26S соотношение фермент/субстрат составило 1/1 (по белку, мкг/мкг) или 1/110 (моль/моль). Количество протеасомы оценивали по методу Лоури, используя бычий сывороточный альбумин в качестве стандарта.
Гидролизаты ОБМ, полученные под действием 20S и 26S комплексов из печени аутбредных мышей, были разделены на фракции методом обращенно-фазовой ВЭЖХ на колонке С4 (Waters, DeltaPak, 300 А). Наблюдаются некоторые отличия в профилях элюции, в частности, в некоторых пиках, совпадающих для 20S и 26S протеасом, содержится разное количество вещества, кроме того, при гидролизе 26S протеасомой появляются новые фракции. Таким образом,
паттерн деградации ОБМ 26S протеасомой несколько изменен по сравнению с таковым для 20S протеасомы. Отмеченные различия можно объяснить разной доступностью для протеолиза участков ОБМ, находящихся на поверхности белковой глобулы и в глубине молекулы, а также имеющих выраженную вторичную структуру. Для 26S протеасомы доступность разных участков ОБМ не имеет большого значения, поскольку в составе 19S субчастицы есть субъединицы, отвечающие за денатурацию молекул белка, которые будут подвергнуты деградации.
Пул протеасом неоднороден и состоит из макромоле-кулярных комплексов нескольких типов, причем каталитические субъединицы могут относиться к т. н. конститутивным (ßl, ß2 и ß5) или иммунным (ßli, ß2i и ß5i) (рис. 2). Шесть каталитических субъединиц протеасомы обладают тремя типами активности, а именно: химотрипсино-подобной (гидролиз после гидрофобных и ароматических аминокислот Leu, Tyr, Phe), трипсиноподобной (гидролиз после положительно заряженных Lys и Arg) и каспазо-подобной (гидролиз после отрицательно заряженных Asp и Glu) .
Соотношение конститутивная протеасома/иммунопро-теасома имеет ярко выраженную тканеспецифичность и в значительной степени зависит от иммунного статуса организма. Так, например, в головном мозге в норме более 90 % протеасом - конститутивные, а в селезенке около 9095 % протеасом являются иммунопротеасомами. Кроме того, в любых тканях под действием гамма-интерферона интенсивно нарабатываются иммуносубъединицы, которые встраиваются во вновь собранные мультикаталити-ческие комплексы . Ранее было показано, что замены каталитических субъединиц на иммунные приводят к изменению специфичности гидролиза и увеличению его скорости. Иммунопротеасома практически теряет способность
sm ■ . з1 »I Ri- Конститутивная ^ ■Шф Иммуно "шШЖМ TSf"fA qgjMSb-"" Рис. 2. Равновесие протеасома - иммунопротеасома. Иммунные каталитические субъединицы нарабатываются под действием гамма-интерферона Рис. 3. Аминокислотная последовательность ОБМ. Стрелками указаны протео-литические пептиды, определенные с помощью хромато-масс-спектрометрии в гидролизатах ОБМ протеасомой из мозга мышей линии SJL/J (верхняя часть рисунка) и Ва1Ь/С (нижняя часть рисунка). Толщина стрелок обозначает частоту встречаемости соответствующего пептида. Цветными прямоугольниками выделены иммунодоминантные районы ОБМ Рис. 4. Распределение по длинам пептидов, обнаруженных в гидролизатах ОБМ пулами протеасом из мозга мышей линии б) SJL/J. Столбиками на диаграмме представлены экспериментальные значения ионного тока для пептидов данной длины, полученные методом LC-MS масс-спектрометрии гидролизовать пептидные связи после остатков аспарагиновой и глутаминовой кислот (каспазоподобная активность), зато значительно чаще происходит гидролиз после гидрофобных и особенно разветвленных гидрофобных аминокислотных остатков. Таким образом, под действием иммунопротеасомы получается большее количество пептидов, несущих гидрофобные аминокислоты на С-конце. Поскольку С-концевые гидрофобные аминокислоты являются важными якорными фрагментами для связывания с молекулами I класса главного комплекса гистосовместимости, следовательно, изменение в специфичности гидролиза приводит к увеличению выработки пептидов, образующих комплексы с молекулами MHC. Фрагменты, связанные с молекулами МНС, презентируются на внешней мембране клеткам иммунной системы. Таким образом, клетки, содержащие иммунопротеасому, будут более эффективно презентировать свои антигены. Кроме того, известно, что альфа-субъединицы каталитической 20S субчастицы протеасомы действуют как ворота, формируя аксиальный канал, регулирующий вход и выход белков и продуктов их деградации. Закрытие канала может, таким образом, способствовать более полной деградации субстратов, поскольку препятствует выходу частично гидролизованных полипептидов . Было также продемонстрировано , что открывание канала сильно влияет на кинетику протеолиза и распределение по длине гидролитических фрагментов, полученных in vitro. Если канал открыт, то скорость гидролиза увеличивается, но при этом средняя длина получающихся фрагментов также увеличивается на 40 %. Таким образом, более высокая скорость работы иммунопротеасомы должна приводить к более длинным пептидам - продуктам деградации, которые будут лучше связываться с молекулами МНС и, следовательно, более эффективно представляться на поверхности клетки. Известно, что мыши линии SJL генетически предрасположены к развитию экспериментального аутоиммунного энцефаломиелита. Данная патология является животной моделью рассеянного склероза. С помощью иммуноблоттинга мы изучили состав пула протеасом в головном мозге мышей этой линии и показали, что содержание иммунопротеасом повышено по сравнению с мышами линии Balb/C (данные не приведены). Поэтому на следующем этапе из мозга мышей линии Balb/C и линии SJL была выделена 26S протеасома и изучен протеолиз ОБМ этими образцами протеасом. Гидролизаты ОБМ, полученные под действием протеасом, выделенных из мозга мышей этих двух линий, были исследованы методом LC-MS (высокоэффективная жидкостная хроматография с детекцией методом масс-спектрометрии). На рис. 3 приведена последовательность основного белка миелина с указанием мажорных фрагментов, продуцируемых пулами протеасом из разных источников. Толщина соответствующих стрелок демонстрирует относительное количество пептида в гидролизате при анализе. В аминокислотной последовательности ОБМ выделяют следующие области, соответствующие иммунодоминант-ным районам белка: 12-31, 82-98, 110-128 и 144-169, причем фрагмент 85-98 представляет собой т.н. энцефалитогенный эпитоп. Необходимо отметить, что деградация ОБМ протеасо-мой из печени аутбредных мышей, как полным комплексом, так и каталитической частью, не приводила к выщеплению иммуногенных пептидов, все они подвергались дальнейшей фрагментации внутри каталитической камеры протеасомы. В гидролизате ОБМ протеасомой из мозга мышей обеих линий практически единственным сайтом гидролиза, где протеасома проявляла свою каспазоподобную активность, была связь между аминокислотными остатками Asp81-Glu82, близкая к началу энцефалитогенного пептида. Характер гидролиза ОБМ протеасомами, выделенными из головного мозга мышей линии SJL и Balb/C, был различен. У мышей аутоиммунной линии генерируемые эпитопы существенно лучше колокализуются с иммунодоминантны-ми фрагментами белка. При действии данного пула на ОБМ содержание фрагмента энцефалитогенного пептида составляет до четверти всех получаемых фрагментов гидролиза. У мышей стандартной линии Balb/C - в два раза меньше. Кроме того, полученные фрагменты существенно хуже соотносятся с областями узнавания комплексов гистосовместимости второго класса. На рис. 4 представлено распределение по длинам пептидов в соответствующих гидролизатах. По оси ординат представлены экспериментальные значения ионного тока для пептидов данной длины, полученные методом LC-MS. Из рисунка видно, что максимум распределения приходится на пептиды длиной 8 аминокислот в случае протеасом из головного мозга мышей как линии SJL, так и Balb/C. Однако относительное значение среднего ионного тока в мак- симуме сильно различается, что свидетельствует о существенно большем количестве фрагментов данной длины в случае мышей аутоиммунной линии. В гидролизатах превалируют пептиды с четным числом аминокислотных остатков, ни в одном из них не было обнаружено пептидов короче четырех аминокислотных остатков. Эти данные согласуются с описанными в литературе , а также с тем, что одной из главных ролей протеасомы в клетке является генерация пептидов для последующей презентации на молекулах МНС I класса, на которые могут загружаться пептиды длиной до 10 аминокислотных остатков. Присутствующие в гидролизатах более длинные пептиды могут затем расщепляться до фрагментов меньшей длины и представляться на молекулах МНС I класса, а также участвовать в презентации на молекулах МНС II класса . Таким образом, в настоящей работе показано, что 20S и 26S протеасомы способны гидролизовать основной белок миелина, при этом молярное соотношение протеасома/ОБМ составило 1 /14.5 для 20S и 1/110 для 26S, время полного гидролиза 45 мин и 85 мин соответственно. После разделения гидролизатов методом LC-MS массы фрагментов были определены методом MALDI-масс-спектрометрии, и, после анализа аминокислотной последовательности ОБМ, идентифицированы сайты протеолиза. Нами было продемонстрировано, что основной белок миелина (не подвергавшийся убиквитинилированию) является хорошим субстратом как для 20S, так и для 26S протеасомы. Впервые были определены сайты протеоли-за ОБМ протеасомой из мозга мышей линий Balb/C и SJL и показаны значительные различия в паттерне деградации данного нейроантигена, что может свидетельствовать о лучшей презентации фрагментов основного белка миелина на комплексах гистосовместимости в случае мышей, предрасположенных к развитию экспериментального аутоиммунного энцефаломиелита. Работа была поддержана грантами РФФИ 07-04-12100-офи, 09-04-01546-а, 07-04-92168-НЦНИ_а, NATO SFPP 982833 и программой президиума РАН фундаментальные науки - медицине 2008 г. Список литературы 1. Ponomarenko, N.A., Durova, O.M., Vorobiev, I.I., Aleksandrova, E.A., Telegin, G.B., Chamborant, O.A., Sidorik, L.L., Suchkov, S.V., Alekberova, Z.S., Gnuchev, N.V., Gabibov, A.G. // J. Immunol. Methods, 2002. V. 269, P. 197- 211. 2. Ponomarenko, N. A., Durova, O. M., Vorobiev, I. I., Belogurov, A. A., Telegin, G. B., Suchkov, S. V., Kiselev, S. L., Lagarkova, M. A., Govorun, V. M., Serebryakova, M. V., Gabibov, A.G. // Proc. Natl. Acad. Sci. USA 2006. V. 103, P. 281-286. 3. Belogurov, A.A. Jr., Kurkova, I.N., Friboulet, A., Thomas, D., Misikov, V.K., Zakharova, M.Y., Suchkov, S.V., Kotov, S.V., Alehin, A.I., Avalle, B., Souslova, E.A., Morse, H.C. 3rd., Gabibov, A.G., Ponomarenko, N.A. // J. Immunol., 2008. V. 180, P. 1258-1267. 4. Polosukhina, D. I., Kanyshkova, T. G., Doronin, B. M., Tyshkevich, O. B., Buneva, V. N.. Boiko, A. N., Gusev E. I., Nevinsky, G. A., Favorova, O. O. // Immunol Lett., 2006. V. 103, P. 75-81. 5. Белогуров, А. А., Куркова, И. Н., Мисиков, В. К., Сучков, С. В., Телегин, Г. Б., Алехин, А. И., Гончаров, Н. Г., Кнорре, В. Д., Габибов, А. Г., Пономаренко, Н. А. // Доклады Академии Наук, 2007. Т. 413, С. 408-411. 6. Pritzker, L. B., Joshi, S., Gowan, J. J., Harauz, G., Moscarello, M. A., // Biochemistry, 2000. V. 39, P. 5374-5381. 7. Schaecher, K. E., Shields, D. C., Banik. N. L. // Neurochemical Research, 2001. V. 26, P 731-737. 8. Medveczky, P., Antal, J., Patthy, A., Kekesi, K., Juhasz, G., Szilagyi, L., Graf, L. // FEBS Lett, 2006. V. 580, P 545-552. 9. D"Souza, C. A., Moscarello, M. A. // Neurochem Res, 2006. V. 31, P 1045-1054. 10. Tewari, M. K., Sinnthamby, G., Rajagopal, D., Eiseinlohr L. C., // Nature Imm, 2005. V. 6, N. 3, P 287-294. 11. Lucas, J., Lobo, D., Terry, E., Hogan, E. L., Banik N. L. // Neurochem. Res., 1992. V. 17, 12. Akaishi, T., Shiomi, T., Sawada, H., Yokosawa, H. // Brain Research, 1996. V. 722, P 139-144 13. Абрамова, Е. Б., Астахова, Т. М., Ерохов, П. А., Шарова, Н. П. // Известия РАН, серия биологическая, 2004. Т. 2, С. 150-156. 14. Orlowski, M., Cardozo, C., Michaud, C. // Biochemistry, 1993. V. 32, P 1563-1572. 15. Namiki, S., Nakamura, T., Oshima, S., Yamazaki, M., Sekine, Y., Tsuchiya, K., Okamoto, R., Kanai, T., Watanabe, M. // FEBS Lett, 2005. V. 579, P. 2781-2787. 16. Kisselev, A. F., Kaganovich, D., Goldberg, A. L. // J. Biol. Chem., 2002. V. 277, P. 22260-22270. 17. Kohler, A., Cascio, P., Leggett, D. S., Woo, K. M., Goldberg, A. L., Finley, D. // Mol. Cell., 2001. V. 7, P. 1143-1152. 18. Mishto, M., Luciani, F., Holzhutter, H.G., Bellavista, E., Santoro, A., Textoris-Taube, K., Franceschi, C., Kloetzel, PM., Zaikin, A. // J. Biol. Chem., 2008. V. 377, P. 1607-1617. 6. БЕЛКИ МИЕЛИНА Белковый состав миелина своеобразен, но существенно проще, чем в нейронах и глиальных клетках. В миелине велика доля катионного белка – КБМ. Он представляет собой относительно небольшой полипептид с М г = 16–18 кД. КБМ содержит значительную долю диаминокислот и в то же время около половины составляющих его аминокислот – неполярные. Это обеспечивает, с одной стороны, тесный контакт с гидрофобными компонентами липидов миелина, а с другой стороны, определяет его способность к образованию ионных связей с кислыми группировками липидов. Необычайно высокой гидрофобностью характеризуются так называемые протеолипидные белки Фолча, составляющие большую часть остальных белков миелина. В свою очередь, главный из этих белков – липофилин, в котором 2/3 составляющих аминокислот – неполярные. Интересна определенная избирательность контактов липофилина с липидами, например, вытеснение холестерина из его окружения. Полагают, что это связано с особенностями вторичной структуры липофилина. Довольна велика также доля так называемого белка Вольфграма – кислого протеолипида, довольно богатого остатками дикарбоновых аминокислот, и, в то же время, содержащего около половины остатков неполярных аминокислот. Наконец, из нескольких десятков других белков миелина отметим миелинассоциированный гликопротеин, расположенный на экстраделлюлярной поверхности мембран; он встречается, кроме того, в олигодендроцитах до миелинизации и в миелине периферической нервной системы. В ЦНС человека он представлен тремя полипептидными цепями с М г =92, 107, 113 кД, а в периферической нервной системе – одним белком с М г =107 кД. МАГ относится к гликопротеинам с относительно низким содержанием углеводных остатков – около 30% от массы молекулы, но содержит характерный для гликопротеинов набор углеводов: N‑ацетилглюкозамин, N‑ацетилнейраминовая кислота, фукоза, манноза и галактоза. Для белковой части молекулы характерно высокое содержание глутаминовой и асларагиновой кислот. Функции белка Вольфграма и МАГ неизвестны, если не считать общих соображений об их участии в организации структуры миелиновых оболочек. 7. НЕЙРОСПЕЦИФИЧЕСКИЕ БЕЛКИ ГЛИИ Белок S‑100 содержится и в нейронах, и в глиальных клетках, причем доля его в последних велика – около 85%. В 1967 г. из а 2 -глобулинов мозга был выделен нейроспеци-фический а 2 -гликопротеин с молекулярной массой 45 кД. В мозге человека он появляется на 16‑й неделе эмбрионального развития. Углеводные компоненты его включают глюкозамин, маннозу, глюкозу, галактозу, галактозамин и N‑ацетилнейраминовую кислоту. а 2 -гликопротеин локализован только в астроцитах, но отсутствует в нейронах, олигодендроцитах и в клетках эндотелия. Поэтому его можно рассматривать как один из специфических маркеров астроцитов. Другой белок опять-таки характерен только для клеток глии. Он был выделен из богатых фиброзными астроцитами областей головного мозга человека, а впоследствии – в значительно больших количествах – из мозга больных множественным склерозом. Это вещество было названо глиальным фибриллярным кислым белком. Он специфичен только для ЦНС, а в ПНС он не обнаружен. Содержание его в белом веществе головного мозга превышает таковое в сером веществе. В онтогенезе мышей максимальное содержание GFA наблюдается между 10‑м и 14‑м днями постнатального развития, т.е. совпадает по времени с периодом миелинизации и пиком дифференцировки астроцитов. Молекулярная масса белка составляет 40–54 кД. Глиальная локализация этого белка также позволяет использовать его как «маркерный» белок для этих клеток. Функции а 2 -гликопротеина и белка GFA неизвестны. Что касается белков микроглии, то следует иметь в виду участие этих клеток в построении миелина. Многие из белков миелина, выявлены в микроглии. В глии представлены также многие рецепторные и ферментные белки, участвующие в синтезе вторичных мессенджеров, предшественников нейромедиаторов и других регуляторных соединений, которые могут быть отнесены к нейроспецифическим. 8. ИНТЕНСИВНОСТЬ МЕТАБОЛИЗМА БЕЛКОВ В РАЗЛИЧНЫХ ОТДЕЛАХ НЕРВНОЙ СИСТЕМЫ Современное представление о динамическом состоянии белков в нервной ткани было установлено благодаря применению изотопов А.В. Палладиным, Д. Рихтером, А. Лайтой и другими исследователями. Начиная с конца 50‑х и в течение 60‑х годов при изучении метаболизма белка использовались различные предшественники их биосинтеза, меченые С, Н, S. При этом было показано, что белки и аминокислоты в головном мозге взрослого животного метаболируют, в общем, более интенсивно, чем в других органах и тканях. Например, в опытах in vivo при применении в качестве предшественника равномерно меченой С‑1–6‑глюкозы оказалось, что по интенсивности образования аминокислот за счет глюкозы ряд органов можно расположить в следующем порядке: головной мозг > кровь > печень > селезенка и легкие > мышца. Аналогичная картина наблюдалась при использовании и других меченых предшественников. Показано, что из С-ацетата в головном мозге интенсивно синтезируется углеродный скелет аминокислот, особенно моноаминодикарбоновых кислот и прежде всего глутамата; из моноаминомонокарбновых кислот достаточно интенсивно образуются глицин, аланин, серии и др. Следует отметить, что особое место в метаболизме аминокислот занимает глутамат. В опытах in vitro с использованием меченого глутамата показано, что если в реакционную среду гомогената мозга добавить только одну глутаминовую кислоту, то она может быть источником образования 90–95% аминокислот. Были проведены многочисленные исследования по изучению различий в интенсивности метаболизма суммарных и индивидуальных белков с помощью меченых предшественников. В опытах in vivo при использовании С-глутамата было показано, что он включается в 4–7 раз интенсивнее в белки серого вещества, чем белого. Во всех случаях интенсивность обмена суммарных белков серого вещества больших полушарий мозга и мозжечка оказалась значительно выше, чем белого вещества тех же отделов мозга, какой бы предшественник ни применялся при исследовании. При этом различие интенсивности обмена суммарных белков серого вещества по сравнению с белками белого вещества имеет место не только в норме, но, как правило, и при различных функциональных состояниях организма. Проводились также исследования по изучению различий в интенсивности включения меченых предшественников в суммарные белки центральной и периферической нервной систем. Оказалось, что несмотря на существенные различия в составе, метаболизме и функциональной деятельности различных отделов ЦНС и ПНС, а также на сложность и гетерогенность белков, входящих в их состав, суммарные белки ЦНС взрослых животных обновляются значительно интенсивнее, чем суммарные белки ПНС. Много исследований посвящено метаболизму белков в различных отделах головного мозга. Например, при изучении распределения радиоактивности в головном мозге после введения С-глутамата оказалось, что на долю серого вещества больших полушарий приходится 67,5 радиоактивности, мозжечка – 16,4, продолговатого мозга – 4,4, на долю других отделов головного мозга – около 11,7. В опытах in vivo при введении взрослым животным различных предшественников, а именно С-глутамата, С‑1–6‑глюкозы, С‑2‑ацетата, оказалось, что по интенсивности включения метки в суммарные белки различные отделы нервной системы располагаются в такой последовательности: серое вещество больших полушарий и мозжечка > таламус > зрительный бугор > средний и промежуточный мозг > Варолиев мост > продолговатый мозг > белое вещество больших полушарий и мозжечка > спинной мозг > седалищный нерв > миелин. Проводились также исследования, посвященные изучению интенсивности обмена белков в различных отделах ЦНС с использованием авторадиографического метода. Получена аналогичная картина: наиболее интенсивное включение метки имело место в белках серого вещества больших полушарий и мозжечка, медленное – в спинном мозге и еще более медленное – в белках седалищного нерва. Что же касается подкорковых образований, то интенсивность обмена их белков была средней между скоростью обновления белков серого и белого вещества больших полушарий и мозжечка. Между отдельными подкорковыми образованиями наблюдаются менее существенные различия, чем между метаболической активностью белого и серого вещества. Исследовались также суммарные белки различных областей коры больших полушарий – лобной, височных, теменной и затылочной. По данным Вэлша и ВАПалладина, более высокой обновляемостью обладают белки сенсорной области коры, а более низкой – белки височной доли коры больших полушарий. Эти же авторы показали, что более высокая обновляемость белков характерна для филогенетически более молодых и функционально более активных структурных образований мозга. На фоне, в общем, высокой обновляемое белков мозга особого упоминания заслуживают немногие довольно инертные белки. К ним относятся гистоны нейронов неокортекса-катионные белки хроматина этих клеток. Во взрослом организме нейроны-неокортекса не размножаются. В соответствии с этим темп обновления гистонов очень незначителен. Среднестатистические сроки обновления половины молекул некоторых фракций гистонов измеряются десятками суток. В головном мозге отсутствуют абсолютно инертные белки, а индивидуальные белки и белковые комплексы нейронов претерпевают непрерывную перестройку, связанную с их участием в функциональной деятельности нейронов и нейроглии. Помимо синтеза и распада целых белковых молекул происходят изменения в их структуре, происходящие, в частности, при аминировании и дезаминировании белков мозга. Их следует рассматривать как частичное обновление отдельных фрагментов белковой молекулы. 1. В нервной ткани обнаружены характерные только для нее нейроспецифические белки. По химической природе они могут быть кислыми или основными, простыми или сложными, часто они представляют собой гликопротеины или фосфопротеины. Многие нейроспецифические белки имеют субъединичную структуру. Число открытых нейроспецифических белков уже превысило 200 и быстро возрастает. 2. Нейроспецифические белки прямо или косвенно участвуют в осуществлении всех функций нервной системы – генерации и проведении нервного импульса, процессах переработки и хранении информации, синаптической передаче, клеточном узнавании, рецепции и др. 3. По локализации в ткани нервной системы различают исключительно или преимущественно нейрональные и глиальные нейроспецифические белки. По субклеточной локализации они могут быть цитопяазматическими, ядерными или мембрано-связанными. Особое значение имеют нейроспецифические белки, локализованные в мембранах синаптических образований. 4. Многие кислые кальиий связывающие нейроспецифические белки участвуют в процессах транспорта ионов. Предполагается, что, в частности, они играют значительную роль в формировании памяти. 5. Особую группу нейроспецифических белков представляют сократительные белки нервной ткани, которые обеспечивают ориентацию и подвижность цитоструктурных образований, активный транспорт ряда компонентов нейрона и участвуют в нейромедиаторных процессах в синапсах. 6. К группе нейроспецифических белков, связанных с гуморальной регуляцией, осуществляемой головным мозгом, относятся некоторые гликопротеины гипоталамуса, а также нейрофизины и подобные им белки, являющиеся носителями пептидных регуляторов. 7. Разнообразные нейроспецифические гликопротеины участвуют в формировании миелина, в процессах клеточной адгезии, нейрорецепции и взаимном узнавании нейронов в онтогенезе и при регенерации. 8. Ряд нейроспецифических белков представляет собой мозговые изоэнзимы известных ферментов, например енолазы, альдолазы, креатинкиназы и др. 9. Многие нейроспецифические белки весьма активно метаболируют в головном мозге животных, причем интенсивность метаболизма различна в разных отделах мозга и зависит от функционального состояния нервной системы. В целом по интенсивности обновления белки мозга значительно превосходят белки других тканей и органов. Нервная система выполняет важнейшие функции в организме. Она отвечает за все действия и мысли человека, формирует его личность. Но вся эта сложная работы была бы невозможна без одной составляющей — миелина. Миелин – это вещество, образующее миелиновую (мякотную) оболочку, которая отвечает за электроизоляцию нервных волокон и скорость передачи электрического импульса. Главная клетка нервной системы – нейрон. Тело нейрона называется сома. Внутри нее находится ядро. Тело нейрона окружено короткими отростками, которые называются дендриты. Они отвечают за связь с другими нейронами. От сомы отходит один длинный отросток – аксон. Он несет импульс от нейрона к другим клеткам. Чаще всего на конце он соединяется с дендритами других нервных клеток. Всю поверхность аксона покрывает миелиновая оболочка, которая представляет собой отросток клетки Шванна, лишенный цитоплазмы. По сути, это несколько слоев клеточной мембраны, обернутые вокруг аксона. Шванновские клетки, обволакивающие аксон, разделяются перехватами Ранвье, в которых отсутствует миелин. Основными функциями миелиновой оболочки являются: Нервные клетки изолированы благодаря своей оболочке, но все же взаимосвязаны между собой. Участки, в которых клетки соприкасаются, называются синапсы. Это место, где встречаются аксон одной клетки и сома или дендрит другой. Электрический импульс может передаваться внутри одной клетки или от нейрона к нейрону. Это сложный электрохимический процесс, который основан на перемещении ионов через оболочку нервной клетки. Изменение напряжения из-за движения ионов калия и натрия называется «потенциал действия». Он распространяется медленно, но миелиновая оболочка, обволакивающая аксон, ускоряет это процесс, препятствуя оттоку и притоку ионов калия и натрия из тела аксона. Проходя через перехват Ранвье, импульс перескакивает с одного участка аксона на другой, что и позволяет ему двигаться быстрее. После того, как потенциал действия пересекает разрыв в миелине, импульс останавливается, и возвращается состояние покоя. Такой способ передачи энергии характерен для ЦНС. Что касается вегетативной нервной системы, в ней часто встречаются аксоны, покрытые малым количеством миелина или вообще не покрытые им. Скачки между шванновскими клетками не осуществляются, и импульс проходит гораздо медленнее. Миелиновый слой состоит из двух слоев липидов и трех слоев белка. Липидов в нем гораздо больше (70-75%): Белковые слои тоньше липидных. Содержание белка в миелине – 25-30%: Существуют простые и сложные белки нервной ткани. Липиды играют ключевую роль в строении мякотной оболочки. Они являются структурным материалом нервной ткани и защищают аксон от потери энергии и ионных потоков. Молекулы липидов обладают способностью восстанавливать ткани мозга после повреждений. Липиды миелина отвечают за адаптацию зрелой нервной системы. Они выступают в роли рецепторов гормонов и осуществляют коммуникацию между клетками. Немаловажное значение в строении миелинового слоя имеют молекулы белков. Они наряду с липидами выступают в роли строительного материала нервной ткани. Их главной задачей является транспортировка питательных веществ в аксон. Также они расшифровывают сигналы, поступающие в нервную клетку и ускоряют реакции в ней. Участие в обмене веществ – важная функция молекул белка миелиновой оболочки. Наиболее частыми причинами разрушения мякотной оболочки являются: Демиелинизирующие заболевания центральной нервной системы: Демиелинизирующие заболевания периферической нервной системы: Это лишь часть заболеваний, возникающих из-за разрушения миелинового слоя. Симптомы в большинстве случаев схожи. Точный диагноз можно поставить лишь после проведения компьютерной или магнитно-резонансной томографии. Немаловажную роль в постановке диагноза играет уровень квалификации врача.
Заболевания, связанные с разрушением мякотной оболочки, очень сложно лечить. Терапия направлена в основном на купирование симптомов и остановку процессов разрушения. Чем раньше диагностировано заболевание, тем больше шансов остановить его течение. Благодаря своевременному лечению можно запустить процесс восстановления миелина. Однако, новая миелиновая оболочка не будет так же хорошо выполнять свои функции. Кроме того, болезнь может перейти в хроническую стадию, а симптомы сохранятся, лишь слегка сгладятся. Но даже незначительная ремиелинизация способна остановить ход болезни и частично вернуть утраченные функции. Современные лекарственные средства, направленные на регенерацию миелина более эффективны, но отличаются очень высокой стоимостью. Для лечения заболеваний, вызванных разрушением миелиновой оболочки, используются следующие препараты и процедуры: В настоящее время лечение демиелинизации не дает стопроцентного результата, но учеными активно ведутся разработки лекарственных средств, направленных на восстановление мякотной оболочки. Исследования проводятся по следующим направлениям: Возможно, в скором времени заболевания, связанные с разрушением миелина, перестанут быть неизлечимыми. 1. Нейроспецифические
белки
Основной белок миелина Нейронспецифическая енолаза Нейротропин-3 и нейротропин-4/5 Нейротрофический фактор головного мозга Цилиарный нейротрофический фактор Фосфорилированный нейрофиламент Н Пигментный фактор эпителиального происхождения Глиальный фибриллярный кислый протеин 2. Болезнь Альцгеймера
Рецептор конечных продуктов гликозилирования Никастрин . β-амилоид Chlamydia pneumoniae Мелатонин и мелатонин сульфат Серотонин Диагностическая значимость определения аутоантител к гликолипидам
при периферических НП Антитела к миелинасcоциированному гликопротеину Антитела к сульфатированному глюкуронат параглобозиду Антитела к ганглиозидам Антитела к ганглиозиду М1 Антитела к ганглиозиду GD1b Антитела к ганглиозиду GQ1b Антитела к интерферону β Антитела к сфингомиелину Антитела к ламинину β Антикохлеарные антитела Анти-нейрональные аутоантитела Антитела к рибосомальным белкам P и РНК БА - болезнь
Альцгеймера ДНП - демиелинизирующая
нейропатия НП - нейропатия НСБ -
нейроспецифические белки ПНС - периферическая
нервная система СМЖ - спинно-мозговая
жидкость ЦНС - центральная
нервная система NGF - фактор роста
нервов Методы
нейровизуализации и электрофизиологического обследования являются традиционными
для диагностики состояний, связанных с повреждением тканей мозга. В последнее
время все больше внимания привлекает лабораторная диагностика, включающая
определение нейроспецифических белков (НСБ) - биологически активных молекул,
специфичных для нервных тканей и выполняющих функции, характерные для нервной
системы. За последние 30 лет охарактеризовано более 60 различных НСБ мозга. Их
можно классифицировать по локализационно-структурному принципу (нейрональные,
глиальные; мембраноассоциированные и цитоплазматические и т.д.), по
функциональной роли, а также выделяют подгруппу НСБ, прис утствующих в норме и
при патологиях. Определение уровня НСБ способствует ранней диагностике, т.к.
значимые изменения их концентрации часто проис ходят раньше, чем те повреждения,
которые можно выявить методами инструментального обследования. Кроме того, они
позволяют проводить оценку прогноза течения и исхода заболевания, осуществлять
мониторинг лечения пациента.
МВР
выделяется в спинно-мозговую жидкость (СМЖ) при любом повреждении нервной
ткани. Уровень МВР повышается при травмах ЦНС, опухолях, рассеянном склерозе,
подостром склерозирующем панэнцефалите, вирусных энцефалитах, других
неврологических расстройствах. Также уровень MBP повышается в течение
нескольких дней после инсульта и отражает деструкцию миелиновых оболочек.
Предполагают, что выделяемый в СМЖ МВР не идентичен с тем, который находится в
ткани. NSE
является нейроспецифическим маркером. Относится к внутриклеточным ферментам
ЦНС, что позволяет использовать NSE для определения постишемических повреждений
мозга. Однако NSE может повышаться и при некоторых других неврологических
процессах (эпилепсия, субарахноидальное кровоизлияние). Является также маркером
мелкоклеточного рака легкого, нейробластомы. S-100
является специфическим белком астроцитарной глии, способным связывать кальций.
Свое название белок получил благодаря свойству оставаться в растворенном состоянии
в насыщенном растворе сульфата аммония. Семейство белков S-100 состоит из 18
тканеспецифичных мономеров. Два из мономеров: α и β, образуют гомои
гетеродимеры, присутствующие в высокой концентрации в клетках нервной системы.
S-100(ββ) присутствует в высоких концентрациях в глиальных и шванновских
клетках, гетеродимер S100(αβ) находится в глиальных клетках, гомодимер
S-100(αα) - в поперечнополосатых мышцах, печени и почках. S-100
метаболизируется почками, его время полураспада составляет 2 часа. Астроглиальные
клетки - это наиболее многочисленные клетки в мозговой ткани. Они образуют
трехмерную сеть, которая является опорным каркасом для нейронов. Увеличение
концентрации S-100(αβ) и S-100(ββ) в СМЖ и плазме является маркером повреждения
головного мозга. У пациентов с повреждениями мозга при раннем определении
содержание S-100В отражает степень повреждения мозга. Исследования S-100
полезны как для мониторинга, так и для определения прогноза течения
заболевания. Субарахноидальное
кровоизлияние ведет к значительному увеличению уровня S-100 в СМЖ. Следует
отметить, что при этом концентрация белка в плазме остается низкой.
Концентрация S-100 значительно повышается в плазме у пациентов, оперированных в
условиях искусственного кровообращения. Пик концентрации приходится на
окончание экстракорпоральной циркуляции и затем уменьшается в неосложненных
случаях. Замедление снижения концентрации S-100 у пациента в послеоперационный
период говорит о наличии осложнений и повреждении клеток мозга. Раннее
определение и контроль уровня S-100, а также одновременные исследования S-100 и
NSE позволяют выявить и подтвердить наличие повреждений мозга на ранней стадии,
когда возможно успешное лечение. Тест S-100 также можно использовать для
прогноза неврологических осложнений при обследовании пациентов с остановкой
сердца. Повышение
S-100 в сыворотке крови и СМЖ при нарушениях мозгового кровообращения
обусловлено активацией микроглии. Было показано, что в ранней фазе
церебрального инфаркта микроглиальные клетки в периинфарктной зоне
экспрессируют S-100 и активно пролиферируют, причем белки экспрессируются не
более трех дней после инфаркта. Это говорит о том, что активация постоянной
популяции микроглии является ранним ответом мозговой ткани на ишемию и может
быть использована как ранний маркер повреждения. Результаты
исследования S-100 можно использовать для предсказания возможного развития
различных симптомов при черепно-мозговых травмах, состояниях после ушибов и
сотрясений головного мозга. Следует учитывать, что концентрация белка S-100
значительно увеличивается с возрастом, причем у мужчин в большей степени, чем у
женщин. S-100
является один из самых ранних НСБ в формирующемся мозге. Он обнаруживается уже
на 3 месяце пренатального периода в мосте, среднем мозге, мозжечке и затылочной
доле, а к 6 месяцу наблюдается синтез белка во фронтальной коре. Функции ЦНС, в
которых участвует S-100, начинают появляться на 12-15 неделе эмбриогенеза, и к
моменту рождения они уже хорошо сформированы. Ряд исследований показывает
участие этого белка в регуляции обучения и запоминания. Белок
S-100 повышается в период и после обратимого ухудшения внутриутробного
состояния при развитии гипоксии. Его концентрация в различных биологических
жидкостях повышается за 48-72 ч до того, как какая-либо стандартная процедура
отражает церебральные нарушения или гибель плода. Показана высокая значимость
определения S-100B в амниотической жидкости для прогноза внутриутробной гибели
плода (рис.): при уровне cut-o
ff
1,19 мкг/л чувствительность теста составляет
90,9%, специфичность - ~100%.
Уровень
S-100B в пуповинной крови может быть использован для оценки задержки
внутриутробного развития плода (IUGR) (рис.). У
новорожденных показана строгая корреляция между уровнем S-100 и степенью
тяжести внутрижелудочковых кровоизлиянияй (IVH) (рис.) Уровень
S-100В в первые 72 ч жизни у доношенных новорожденных с асфиксией при родах
является достоверным маркером прогноза развития и тяжести церебральных
нарушений. S-100
(αβ+ββ) может определяться как дополнительный диагностический и прогностический
маркер при злокачественной меланоме. Семейство
нейротропинов включает: фактор роста нервов (NGF), нейротрофический фактор
головного мозга (BDNF), NT3 и NT4/5. Они поддерживают различные популяции
нейронов в ЦНС и ПНС. NT - это секретируемые белки, выявляемые в кровотоке,
которые способны подавать отдельным клеткам сигналы на выживание,
дифференцировку или рост. NT действуют, предотвращая инициацию апоптоза в
нейроне. Они также индуцируют дифференцировку клеток-предшественников,
образование нейронов. NT играют важную роль в функционировании нервной системы,
в регенерации поврежденных нейрональных структур. Хотя
в мозге млекопитающих подавляющее большинство нейронов формируются в процессе
эмбрионального развития, мозг взрослых частично сохраняет способнос ть к
нейрогенезу - образованию новых нейронов из нейрональных стволовых клеток. NT
контролируют и стимулируют этот процесс. Трофные (обеспечение выживаемости) и
тропные (направление роста аксонов) свойства NT служат основанием для их
возможного использования в лечении различных типов нейродегенеративных
заболеваний, таких как болезни Альцгеймера, Паркинсона и Гентингтона, а также
периферических нейропатий различного генеза. NT3
- это фактор роста с м.м. 13,6 кДа (м.м. активной формы-димера - 27.2 кДа). NT3
играет роль в развитии симпатической нервной системы. У мышей повышенные уровни
NT3 выявлены в симпатических ганглиях и органах при гипериннервации и при
спонтанной гипертензии. У пациентов, страдающих астмой, кортикостероиды
повышают уровень NT3 в сыворотке. Концентрация NT3 во фронтальном и
париетальном участках коры значительно снижена у больных шизофренией. NT3
способен стимулировать наибольшее количество популяций нейронов, т.к. он
активирует два из трех тирозинкиназных рецепторов NT (TrkC и TrkB). NT4/5
предупреждает гибель двигательных нейронов в перинатальном и постнатальном
периодах. Воздействие NT4/5 осуществляется в основном через TrkB
тирозинкиназный рецептор. Зрелая
молекула BDNF млекопитающих имеет м.м. 13 кДа и состоит из 119 аминокислотных
остатков. BDNF по аминокислотному составу на 52% идентичен NGF. В растворе
существует в виде гомодимера. BDNF экспрессируется в фибробластах, астроцитах,
нейронах различного фенотипа и локализации, мегакариоцитах/тромбоцитах,
шванновских клетках (в районах повреждения) и, возможно, в клетках гладкой
мускулатуры. BDNF в плазме обнаруживается в количествах порядка пг/мл, в то
время как в сыворотке он присутствует в количествах порядка нг/мл. Разница
обуславливается высвобождением BDNF при дегрануляции тромбоцитов и свертывании
крови. Идентичность структуры BDNF у разных млекопитающих потенциально
позволяет использовать данную тест-систему для разных видов животных. Известно,
по меньшей мере, 2 типа рецепторов к BDNF, первые - низкоафинные рецепторы NGF
с м.м. 75 кДа (LNGFR), вторые - высокоафинные рецепторы к тропомиозинкиназе-В с
м.м 145 кДа (TrkB). Извеcтно, что LNGFR может усиливать передачу сигналов по
определенным путям. Биологическое значение активации данных путей изучено
плохо. LNGFR могут участвовать в миграции шванновских клеток в область
повреждения и/или модулировать активность TrkB на клетках, экспрессирующих
одновременно оба рецептора. TrkB обладает способностью связывать NT3 и 4.
Считается, что для работы рецепторов TrkB требуется их гомодимеризация, в то
время как имеются данные об образовании функциональных гетеродимеров молекул
рецепторов TrkB и TrkC на клетках, экспрессирующих оба эти рецептора
одновременно. К таким клеткам относят гранулярные нейроны мозжечка и клетки
дентального ядра гиппокампа. Имеются данные об экспресcии TrkB на мотонейронах
спинного мозга, пирамидальных клетках гиппокампа, почти всех клетках развивающегося
мозга, а также на тимоцитах, что указывает на роль BDNF в лимфопоэзе. Функциональная
активность BDNF довольно велика. В период развития он участвует в
дифференцировке нейронов, созревании, выживании и формировании синапсов. Во
взрослом организме основная функция BDNF - нейропротекция, защита нейронов
головного мозга от ишемических атак и мотонейронов от гибели, индуцируемой
удалением аксонов. Человеческий
CNTF представляет собой одноцепочечный полипептид из 200 аминокислотных
остатков с м.м. 22,7 кДа. Молекула высококонсервативна у различных видов. При
сравнении аминокислотных последовательностей CNTF человека, крысы и кролика
обнаружена гомологичность 83 и 87%, соответственно. CNTF локализован в шванновских
клетках и астроцитах 1 типа. CNTF
относится к ограниченному семейству нейропоэтических цитокинов, включающему
ингибирующий фактор лейкемии (LIF) и онкостатин М (OSM). CNTF рассматривается
как ключевой фактор дифференцировки для развивающихся нейронов и глиальных
клеток. CNTF обеспечивает трофику и участвует в защите поврежденных или
аксонотомированных нейронов. В частности, гибель мотонейронов после аксотомии
лицевого нерва крысы предотвращалась нанесением CNTF на проксимальный
аксональный сегмент. CNTF продемонстрировал in vitro индукцию холинэргических
свойств в адренэргических симпатических мотонейронах. Данное влияние включало
экспрессию ацетилхолина в качестве нейромедиатора и синтез вещества Р (SP) и
вазоактивного интестинального пептида (VIP) в качестве
ацетилхолин-ассоциированных нейропептидов. Влияние CNTF на неавтономные
сенсорные нейроны менее изучено. Обнаружено, что клетки дорзального корешкового
ганглия in vivo увеличивают экспрессию SP, в то время как экспрессия SP и VIP
не увеличивается в ответ на CNTF in vitro. Кроме того, CNTF предположительно
участвует в дифференцировке глии. Другие эффекты CNTF включают: обеспечение
полипотентности эмбриональных стволовых клеток, индукцию выживания и
дифференцировки хромаффинных клеток надпочечника и, подобно ИЛ-6, индукцию
лихорадки после внутривенных инъекций. Интерес к изучению CNTF вызван его
свойством способствовать выживанию нейронов. pNF-H
- чувствительный маркер повреждений аксонов. Нейрофиламенты составляют основную
часть цитоскелета нейронов. Тремя основными белками нейрофиломентов являются
NF-L, -M и -H. Особенно высока их концентрация в аксонах. Белок NF-H обладает
некоторыми уникальными свойствами. В аксональных нейрофиламентах сериновые
остатки этого белка, содержащиеся в повторах лизин-серин-пролин, сильно
фосфорилированы. Фосфорилированные формы NF-H (рNF-H) устойчивы к действию
протеаз после выхода из поврежденных аксонов. Следовательно, определение этого
белка в СМЖ или крови может предоставлять информацию о степени аксонального
повреждения. pNF-H
определяется в образцах сыворотки только при наличии повреждений спинного или
головного мозга. Концентрации pNF-H могут достигать высоких уровней (>250
нг/мл) и возвращаться к нулевому уровню через недели после повреждения. Так как
pNF-H экспрессируется только в аксонах, определение его содержания является
удобным и чувствительным биомаркером оценки аксональных повреждений. Показано,
что рNF-H может быть выявлен в плазме у людей, страдающих невритом зрительного
нерва или в СМЖ у пациентов при злокачественных опухолях мозга или инсульте. PEDF
- это гликопротеин с м.м. ~50 кДа, обладающий множеством биологических функций.
Это нейропротективный и нейротрофический фактор, который воздействует на
различные типы нейронов. Показано, что PEDF является сильным активатором
нейрональной дифференцировки клеток ретинобластомы человека. На птицах и мышах
показано, что он обеспечивает выживание и дифференцировку развивающихся
двигательных нейронов спинного мозга, поддерживает нормальное развитие
фоторецепторного нейрона земноводных и экспрессию опсина в отсутствии клеток
пигментного эпителия сетчатки (RPE). У
крыс PEDF является фактором выживаемости зернистых нейронов мозжечка, защищая
их от апоптоза и нейротоксичности глутамата. Он также защищает двигательные
нейроны и развивающиеся нейроны гиппокампа от дегенерации, индуцированной
глутаматом. На культурах клеток было показано, что он предохраняет нейроны
сетчатки глаза от гибели, индуцированной перекисью. GFAP
является членом семейства белков цитоскелета и представляет собой основной 8-9
нм промежуточный филамент в зрелых астроцитах ЦНС. GFAP - мономерная молекула с
м.м. 40-53 кДа и изоэлектрической точкой 5,75,8. Это высоко специфичный белок
мозга, который не обнаружен за пределами ЦНС. Было показано, что GFAP очень
быстро высвобождается в кровь после травматического повреждения мозга (может
служить маркером тяжести повреждения и прогностическим фактором в отношении
исхода), но при множественной травме без повреждения мозга высвобождения GFAP
не происходит. В ЦНС после повреждения (будь то результат травмы, заболевания,
генетического нарушения или химического инсульта) астроциты в результате
типичного поведения отвечают астроглиозом. Астроглиоз характеризуется быстрым
синтезом GFAP. Известно, что уровень GFAP обычно растет с возрастом. Благодаря
высокой специфичности и раннему высвобождению из ЦНС после травматического повреждения
мозга, GFAP может оказаться очень полезным маркером для ранней диагностики. Болезнь
Альцгеймера (БА) - это прогрессирующее старческое слабоумие, которому
подвержена примерно половина популяции людей старше 85 лет. Признаками этого
заболевания являются потеря памяти и другие аномалии в поведении, которые
коррелируют с потерей нейронов первоначально в коре головного мозга и
гиппокампе. БА характеризуется присутствием внеклеточных бляшек и
внутриклеточных нейрофибриллярных клубков в тканях мозга. RAGE
- это мультилигандный трансмембранный гликопротеин I типа, принадлежащий
суперсемейству иммуноглобулинов (Ig). RAGE предположительно вовлечен в
различные патологические процессы, включая сахарный диабет, болезнь Альцгеймера
(БА), системный амилоидоз и опухолевый рост. RAGE может участвовать в
физиологических функциях, таких, как рост, выживаемость и регенерация нейронов,
провоспалительные реакции. Высокая экспрессия RAGE наблюдается в процессе
развития, особенно в ЦНС. К лигандам RAGE относятся конечные продукты
гликозилирования (AGEs), амилоид-β (Aβ), HMG-1 (также известный как
амфотерицин) и некоторые белки семейства S-100. Aβ - это главный компонент
сенильных, или амилоидных бляшек, одного из ключевых нейроморфологических
признаков БА. RAGE является рецептором для β-складчатых структур, характерных
для амилоида, обнаружено локализованное повышение его уровня вблизи Aβ в мозге
при БА. Взаимодействие Aβ с RAGE, экспрессируемым на эндотелиальных клетках,
нейронах и микроглии приводит к образованию активных форм кислорода и продукции
провоспалительных факторов, что является предполагаемым механизмом, лежащим в
основе нейродегенеративного процесса при БА. Недавние исследования показали
возможность участия RAGE в транспорте Aβ через гематоэнцефалитический барьер и
его накоплении в ЦНС. Показано,
что взаимодействие RAGE со своим лигандом HMG-1 регулирует подвижность клеток.
Например, HMG-1/RAGE способен стимулировать рост аксонов у клеток
нейробластомы. Блокировка связывания HMG-1/RAGE подавляет рост и
метастазирование опухоли в экспериментах у животных. Кроме того, показано, что
концентрации RAGE и S-100 повышаются при рассеянном склерозе и при
экспериментальном аутоиммунном энцефаломиелите (EAE). Никастрин
представляет собой состоящий из 709 аминокислот трансмембранный гликопротеин
типа I, который недавно был описан как ключевой компонент связанного с БА
мультипротеинового комплекса, образованного с протеазами (презенилин-1 и -2).
Формирование этого комплекса является заключительным этапом в образовании
нейротоксичного β-амилоидного пептида (также известного как амилоид), который
можно обнаружить в мозговых бляшках у пациентов, страдающих семейной БА.
Амилоидный белок образуется из связанного с мембраной белка-предшес твенника
β-амилоида (βАРР) в два этапа. Вначале β-АРР расщепляется протеазой
β-секретазой (ВАСЕ-2) и, затем амилоидный белок высвобождается при последующем
γ-секретазном процессинге. Было показано, что презенилины-1 и -2 обладают
протеазной каталитической активностью, которая необходима для образования
нейротоксичного β-амилоидного пептида. Известно, что никастрин связывается с
β-АРР и способен модулировать образование β-амилоидного пептида. Это указывает
на прямую роль никастрина в патогенезе БА и позволяет рассматривать его в
качестве потенциальной мишени для терапевтического вмешательства. Основным
белковым компонентом бляшек при БА является β-амилоид - пептид, состоящий из
40-43 аминокислотных остатков, отщепляемый от белка-предшественника (АРР)
ферментами β-секретазой и, возможно, γ-секретазой. Увеличение
секреции пептидов с большей м.м. (Аβ42 или Аβ43) происходит при определенных
генетических мутациях, при экспрессии некоторых АроЕ аллелей, или при участии
других, пока неизвестных, факторов. Не только протеолитическое расщепление АРР
и последующее появление Аβ могут быть важными факторами прогрессии БА, но и
агрегация Аβ также может иметь критическое значение в развитии этого заболевания,
вести к развитию плотных бляшек, которые обнаруживаются в мозге пациентов с АD.
Показано, что Аβ42 или Аβ43 имеют тенденцию к агрегации в гораздо большей
степени, чем пептиды с меньшей м.м. Показано, что возрастание концентрации
Аβ42/ Аβ43 ведет к абнормальному накоплению Аβ и ассоциировано с
нейротоксичностью в тканях мозга при БА. Для пациентов с БА снижение уровня
Аβ42 в СМЖ является прогностическим фактором. Определение Аβ пептида может
также быть использовано для идентификации человеческого Аβ у мышей при
моделировании БА. Определение различных фрагментов пептидов для изучения
клеточного ответа на воздействие Аβ пептидов может помочь разобраться в ранних
событиях, которые приводят к гибели нервных клеток. Аβ пептиды могут
активировать различные пути сигнальной трансдукции. Например, недавно было
показано, что фибриллярный Аβ активирует тирозинкиназы Lyn и Syk, инициируя
таким образом сигнальный каскад, в результате которого активируются
пролин-богатая/кальций-зависимая тирозинкиназа Pyk2. Учитывая,
что Аβ пептиды имеют тенденцию к агрегации, качество диагностических наборов
может варьировать от производителя к производителю, от лота к лоту. Компания
«BioS ource International» разработала высокочувствительные и высокоспецифичные
ИФА-наборы для количественного определения Аβ 1-40 или 42.
С
помощью ПЦР метода в независимых исследованиях было показано, что 89-92%
пациента с БА имели положительную реакцию на антиген Сh. pneumoniaе (мозг).
Антиген Сh. pneumoniaе был идентифицирован во внеклеточных бляшках в мозге
пациентов с БА, в отличие от мозга пациентов с другими повреждениями мозга,
приводящими к слабоумию. Сh.
pneumoniaе инфицирует моноциты, что приводит к увеличению их миграции через
гемэнцефалотический барьер. Сh. pneumoniaе приводит к нарушению регуляции
β-катепсина, N-кадгерина, VE-кадгерина и других молекул межклеточной адгезии.
При определении антител в сыворотках пациентов с БА и болезнью Паркинсона с
помощью ИФА были получены следующие результаты: Болезнь Альцгеймера: IgA - 45%,
IgG - 36% положительных результатов; Болезнь Паркинсона: IgA - 35%, IgG - 83%
положительных результатов. Показано,
что важную роль в патогенезе БА играет оксидативный стресс (ОС). БА развивается
в пресенильном или старческом возрасте параллельно с усилением ОС. Основными
признаками БА у пациентов на поздних стадиях являются нейрофибриллярные клубки
(NFTs) и β-амилоидные (сенильные) бляшки в коре головного мозга. Многие
исследования показали, что на ранних стадиях у пациентов с БА можно наблюдать
различные признаки ОС - окислительные повреждения нуклеиновых кислот, белков и
липидов, показано также присутствие различных биомаркеров ОС (рис). В настоящий
момент ведутся многочисленные исследования новых терапевтических подходов
предотвращения или замедления развития этого заболевания, основанные на защите
от оксидативного стресса. Эпифиз
является частью центральной системы нейрогуморальной регуляции организма.
Эпифизу принадлежит ведущая роль в передаче информации на все
жизнеобеспечивающие системы организма о смене дня и ночи, а также в организации
сезонных и циркадных ритмов и регуляции репродуктивных функций. Для оценки
функционального состояния эпифиза в настоящее время необходимо определение
мелатонина и серотонина в крови и продуктов метаболизма мелатонина (мелатонина
сульфата) в моче. Мелатонин,
или N-ацетил-5-метокси-триптамин - главный гормон эпифиза. Он синтезируется в
эпифизе из промежуточного метаболита серотонина - N-ацетилсеротонина. Уровень
мелатонина в крови имеет значительные индивидуальные колебания, максимальные
значения мелатонина в крови наблюдаются между полуночью и 4 часами утра.
Регуляция секреции мелатонина находится под контролем симпатической нервной
системы, которая оказывает свое регулирующее влияние посредством норадреналина.
Период полураспада мелатонина составляет 45 мин. Это означает, что для
исследовательских целей образцы крови должны быть собраны через короткие
промежутки времени с целью определения периода в продукции мелатонина. Кроме
того, нарушение сна пациента в течение ночи с целью сбора образцов может
повлиять на уровень мелатонина в крови. Этих проблем можно избежать, если
определять уровни метаболитов мелатонина: мелатонин сульфата
(6-сульфатокимелатонина) и 6-гидроксиглюкуронида в моче. 80-90% мелатонина
секретируется в мочу в виде сульфата. Концентрация мелатонин сульфата в моче
хорошо коррелирует с общим уровнем мелатонина в крови в течение периода сбора
образцов. В
настоящее время физиологическая и патофизиологическая роль мелатонина активно
изучается. Нарушение уровня мелатонина в крови соответствует расстройствам сна,
депрессии, шизофрении, гипоталамической аменорее и некоторым видам
злокачественных новообразований. Преждевременное половое созревание может быть
обусловлено наличием опухоли в эпифизе. Если опухоль развивается из
энзимоактивных элементов паренхимы, то преобладают явления гиперпинеализма или
диспинеализма. Недостаточность секреции мелатонина эпифизом приводит к
повышенной выработке ФСГ и, следовательно, к персистенции фолликула,
поликистозу яичников, общей гиперэстрогении. На этом фоне могут развиваться
фиброматоз матки, дисфункциональные маточные кровотечения. Гиперфункция
эпифиза, наоборот, индуцирует гипоэстрогению, половую фригидность. Повышение
уровня мелатонина в крови и его экскреции с мочой наблюдается у больных с
маниакальными состояниями. Нарушение
продукции мелатонина, как количественно, так и ее ритма является пусковым
моментом, приводящим на начальных этапах к десинхронозу, за которым следует
возникновение органической патологии. Следовательно, сам факт нарушения
продукции мелатонина может являться причиной возникновения различных
заболеваний. Получены данные, позволяющие считать мелатонин одним из наиболее
мощных эндогенных антиоксидантов. Более того, в отличие от большинства других
внутриклеточных антиоксидантов, локализующихся преимущественно в определенных
клеточных структурах, присутствие мелатонина и, следовательно, его
антиоксидантная активность, определены во всех клеточных структурах, включая
ядро. Серотонин
является промежуточным продуктом метаболизма триптофана, образующегося в
основном в энтерохромаффинных клетках тонкого кишечника, в серотонинэргических
нейронах мозга, в тромбоцитах крови. Почти весь серотонин в циркулирующей крови
сконцентрирован в тромбоцитах. Изменение концентрации циркулирующего серотонина
наблюдается при хронической головной боли, шизофрении, гипертензии, болезни Хантингтона,
мышечной дистрофии Дюшена и ранней стадии острого аппендицита. Определение
уровней сывороточного серотонина имеет большое клиническое значение для
диагностической оценки карциноидного синдрома. Полиневропатии
(нейропатии, НП) могут быть классифицированы по этиологии (сосудистые,
аллергические, токсические, метаболические и т.д.) или по клиническим
проявлениям (сенсорные, двигательные, сенсомоторные, мононейропатии и т.д.).
Частыми признаками периферических нейропатий являются слабость и потеря
чувствительности или боли в конечностях. Точная диагностика периферических
нейропатий требует совместного анализа клинических признаков, истории болезни и
лабораторных исследований, которые могут позволить установить, подтвердить,
классифицировать и осуществить мониторинг заболевания. В
последние годы многие гликоконъюгаты рассматривались как предполагаемые мишени
при различных НП. Все чаще и чаще НП характеризуют не только по клиническим и
электрофизиологическим критериям, но и иммунохимически, в зависимости от типа
антигена, распознаваемого антигликолипидными антителами. К гликоконъюгатам
относятся как гликопротеины (например, MAG), так и гликолипиды (например,
ганглиозиды, SGPG, сульфатиды или сульфолипиды). Они содержатся во всех тканях
и являются компонентами миелиновой оболочки нервных волокон. Среди большого
разнообразия гликолипидов к настоящему времени для трех показана важная
клиническая значимость при диагностике НП и выборе лечения (рис.). Выявлена значительная
корреляция между отдельными клиническими особенностями и типами антител к
различным гликоконъюгатам, присутствующими в сыворотке. Главными
мишенями для аутоантител при аутоиммунных периферических НП являются
сульфатированный глюкуронат параглобозид (SGPG) и ганглиозид GM1. Первый
является мишенью в основном при демиелинизирующих НП, ассоциированных с
моноклональными IgM гаммапатиями. Второй является преимущественной мишенью при
двигательных НП, главным образом при мультифокальной моторной нейропатии.
Анти-GQlb IgG антитела характерны для подгруппы пациентов с синдром
Миллера-Фишера, (вариант синдрома Гийена-Барре). Выяснение структуры эпитопа
может также быть важно для определения патологической роли антител. Во
многих случаях высокую значимость имеют раздельные определения IgG и IgM
классов аутоантител, т.к. антитела класса IgG более характерны для острых
невропатий, а IgM антитела чаще присутствуют при хронических состояниях. Структура
и локализация трех основных гликоконъюгатных антигенов на периферических нервах
A. Миелин-ассоциированный гликопротеин, содержащий пять внеклеточных
Ig-подобных доменов, доступных для аутоантител, трансмембранный домен и
цитоплазматический хвост. B. Сульфатированные гликолипиды и ганглиозид GM1, чьи
олигосахаридные цепи расположены близко к липидному бислою миелиновой мембраны. Являются
важным дополнением к методам электродиагностики для выявления различных
подгрупп аутоиммунных НП: различные неврологические симптомы определяются по
профилю антигликолипидных антител. Возможность точной дифференциальной
диагностики НП, в основе которых лежат иммунологические нарушения (например, НП
при моноклональных гаммопатиях, мультифокальная моторная НП или синдром
Гийена-Барре). Контроль терапии НП, связанных с моноклональными гаммапатиями. Проведение научных исследований в области нейроиммунологии. MAG
принадлежит к молекулам клеточной адгезии и экспрессируется на
олигодендроглиоцитах и шванновских клетках. Он является медиатором
взаимодействий олигодендроглиоцитов между собой и с нейронами. При миелинизации
аксонов он также обнаруживается на их внешних поверхностях и прилежащих
поверхностях клеток, формирующих миелин. Более 50% пациентов с периферической
НП и IgM-моноклональной гаммапатией имеют моноклональные IgM-антитела, которые
связываются с MAG. Определение
анти-MAG антител принципиально для дифференциации IgM-ассоциированной НП с
другими обычно встречающимися приобретенными полинейропатиями типа CIDP
(хроническая воспалительная демиелинизирующая НП). Оба нарушения могут медленно
прогрессировать и проявляться при морфологическом и электрофизиологическом
исследованиях преимущественно как демиелинизирующая НП (ДНП). Кроме того, при
этих заболеваниях повышена концентрация белка в СМЖ, и по этому показателю
можно судить об эффективности проведенной иммуносупрессивной терапии. Таблица. Периферические нейропатии, ассоциированные со специфическими аутоантителами
Символы:
Определение уровня титра антител к гликолипидам: (+) -
слабоположительный, + - умеренно положительный, ++ - положительный, +++
-высоко положительный;
.
[%] - процент пациентов, у которых выявляются аутоантитела к гликолипидам.
.
Голубой
цвет ячейки указывает на IgG класс или преобладание IgG
антигликолипидных антител; оранжевый цвет относится к IgM классу.
Пример использования 1:
антитела к GM1 при GBS выявляются часто, в высоких титрах, при этом
преобладает IgG изотип. GM1 IgG выявляются у 20-30% пациентов.
Пример использования 2:
моноклональные антитела IgM к GD1b обычно присутствуют в высоких титрах
при сенсорной атаксической нейропатии и CANOMAD синдроме.
Олигосахаридная
последовательность SGPG с глюкуронилсульфатом (т.е. эпитоп HNK-1) общая для
сульфатированного глюкуроната параглобозида и его производных и белков, главным
образом миелин-ассоциированных белков, миелин-олигодендроцитного гликопротеина
(MOG) в ЦНС и периферического белка миелина (РМР22) в ПНС, изоформы
ацетилхолинэстеразы и подгруппы нескольких молекул адгезии, таких как молекула
адгезии нервных клеток (NCAM). Существует мнение, что вне зависимости от
специфичности белка, IgM анти-SGPG практически всегда выявляются в
биологических образцах при ДНП и при некоторых заболеваниях двигательных
нейронов. Показано, что при типичных сенсорных ДНП выявляются и анти-MAG и
анти-SGPG антитела, тогда как при аксональных НП представлены только моноклональные
IgM-анти-SGPG антитела. У пациентов наблюдается зависимость между титром
антител к эпитопу HNK-1 и степенью демиелинизации. Набор
GanglioCombi предназначен для скрининга в человеческой сыворотке аутоантител,
направленных против ганглиозидов - асиало-GM1, -GM2, -GD1a, -GD1b и -GQ1b.
Ганглиозиды образуют семейство кислых сиалированных гликолипидов, состоящих из
углеводных и липидных компонентов. Они в основном находятся на наружной
поверхности плазматической мембраны. Внешнее расположение углеводных остатков
позволяет предположить, что они служат антигенными мишенями при аутоиммунных
неврологических расстройствах. Антитела, связывающиеся с углеводными
антигенами, обнаружены при различных периферических НП. Наблюдается
значительная гетерогенность экспрессии ганглиозидов в тканях ПНС. GM1 и GD1 в
основном присутствуют на двигательных нервах, GQ1b выявляются в повышенных
количествах в двигательных черепных нервах мышц глазного яблока. Высокая
экспрессия GD1b наблюдается в сенсорных нервах. Показана четкая корреляция
между содержанием специфических анти-ганглиозидных антител и различными
вариантами синдрома ГийенаБарре (GBS). У пациентов с повышенным содержанием
антиганглиозидных антител хороший терапевтический прогноз. Мультифокальная
моторная нейропатия (MMN) характеризуется блокадой проведения импульсов по
аксонам нижних мотонейронов. По клиническим признакам достаточно сложно
провести дифференциацию между MMN и боковым амиотрофическим склерозом (ALS).
Поскольку MMN, в отличие от ALS, является излечимой болезнью, чрезвычайно важно
провести дифференциацию этих болезней на ранней стадии. В то время как высокие
титры анти-GM1 антител практически не обнаруживаются у пациентов с ALS, более
80% пациентов с MMN имеют эти антитела. При MMN рекомендуется одновременное
определение IgG и IgM изотипов анти-GM1 антител. Анти-GM1 антитела встречаются
приблизительно у 5% здоровых людей, особенно у пожилых людей, и их продукция
может быть проявлением нормальной активности иммунной системы. Определение
анти-GM1 антител используется для контроля динамики сероконверсии и
эффективности терапии MMN для предотвращения возможного рецидива заболевания, а
также подтверждения диагноза во всех случаях полинейропатий неизвестного
происхождения. Рекомендуется проведение этого теста у всех пациентов с
моторными нарушениями, и особенно с моторными НП, при синдроме Гийена-Барре
(GBS), при заболеваниях проксимальных нижних мотонейронов. Анализ
анти-GD1b аутоантител может быть полезен для клинической оценки больных
синдромом Гийена-Барре (GBS) без офтальмоплегии (см. также анти-Q1b), при
сенсорных НП, в частности при хронической сенсорной НП больших волокон (крупных
нервных стволов) с атаксией. Анти-GM1 антитела встречаются приблизительно у 5%
здоровых людей, особенно у пожилых людей. Определение анти-GD1b аутоантител
может быть полезно: для проверки пациентов с признаками воспалительной ДНП, но
с отрицательным результатом на анти-GM1 аутоантитела; для контроля
эффективности терапии острых и хронических воспалительных ДНП; как дополнение в
диагностике НП неизвестного происхождения. Рекомендуется выполнять этот анализ
у всех пациентов с моторными нарушениями, и особенно с моторными НП. Синдром
Миллера-Фишера (MFS) в большой степени ассоциирован с присутствием
поликлональных сывороточных IgG-антител к антигену GQ1b, которые могут быть
найдены в сыворотке более чем 90% пациентов с острой стадией MFS. В течение
острой стадии болезни титры антител достигают очень высоких уровней и полностью
исчезают при выздоровлении. У здоровых доноров крови, пациентов с синдромом
Гийена-Барре (GBS) без офтальмоплегии, а также у пациентов с другими
иммунологическими или неврологическими заболеваниями анти-GQIb аутоантитела не
обнаруживаются. MFS - вариант GBS, с которым они имеют перекрывающиеся
клинические и нейрофизиологические признаки. Сходство MFS и GBS недавно было
подтверждено присутствием анти-GQ1b у пациентов с GBS с офтальмоплегией. В
некоторых случаях при MFS могут также обнаруживаться IgAи IgM-аутоантитела,
однако в меньшей степени и только в короткий промежуток времени. Большинство
пациентов, страдающих MFS или GBS с офтальмоплегией и имеющих аутоантитела
против GQ1b, имело в анамнезе инфекцию Campylobacter jejuni. Этот факт
поддерживает гипотезу о молекулярном сходстве между поверхностными эпитопами C.
jejuni и GQ1B, а также то, что MFS инициируется предшествующей C. jejuni
инфекцией. В
последние годы для лечения ремиттирующего рассеянного склероза (RRMS)
используется терапия рекомбинантным интерфероном бета (rIFNβ). Постоянное
продолжительное (от месяца до нескольких лет) введение любого экзогенного
вещества может провоцировать иммунный ответ. У многих пациентов с RRMS,
получавших терапию IFNβ, образуются анти-IFNβ антитела, уменьшающие лечебный
эффект препарата. Показано, что у пациентов с рассеянным склерозом только
небольшая часть антиIFNβ антител способна нейтрализовать иммуномодулирующее
влияние IFNβ. Также показано определение этих антител при сенсорных НП, при
синдроме Гийена-Барре (GBS). СМ
(sphingomyelin) - фосфолипид, в состав которого входит сфингозин, жирная
кислота, фосфорная кислота и холин. СМ - естественный компонент мембран и
липопротеиновых частиц. В больших количествах СМ присутствуют в головном мозге
и нервной ткани. Подавление биосинтеза СМ у лабораторных мышей снижает
плазменные концентрации холестерина (ХС) на 46%, и триглицеридов на 44%, по
сравнению с группой контроля. Кроме того, снижается содержание ХС в частицах
ЛПНП и липопротеинов очень низкой плотности (ЛПОНП) и увеличивается
концентрация ХС липопротеинов высокой плотности (ЛПВП). Исследования на
лабораторных животных показали, что подавление синтеза СМ также приводит к
значительному снижению выраженности атеросклеротического поражения и
макрофагальной инфильтрации. Вероятно, что подавление синтеза сфинголипидов
является перспективным направлением в терапии дислипидемии и атеросклероза.
Антитела к сфинголипидам участвуют в патогенезе аутоиммунной демиелинизации и
обнаруживаются при рассеянном склерозе и аутоиммунном энцефаломиелите. Ламинин
- основной гликопротеин базальных мембран, внеклеточного матрикса, окружающего
эпителиальные ткани, нервы, жировые клетки, гладкие, поперечнополосатые и
сердечные мышцы. Это многофункциональный мультидоменовый гликопротеин с высоким
молекулярным весом состоит из 3 полипептидов - А, В1 и В2, связанных вместе
межцепочечными дисульфидными мостиками. Ламинин способствует адгезии, росту,
миграции и пролиферации клеток, росту нейритов, метастазированию опухолей и,
возможно, клеточной дифференцировке. Известно, что рекомбинантные человеческие
антитела к ламинину блокируют развитие эндотелия сосудов. Потеря
слуха может быть вызвана многими причинами. Некоторые типы тугоухости могут
быть обратимы при условии своевременной диагностики и соответствующем лечении.
Нейросенсорная тугоухость (SNHL), обычно относимая к глухоте, связанной с
поражением нерва, может быть обусловлена генетическими или приобретенными
факторами, такими как инфекции или может быть вызвана иммунологическими
причинами. В большинстве случаев причину SNHL установить не удается. Такие
случаи относят к идиопатической SNHL. Существует подгруппа пациентов с
идиопатической SNHL, с очень хорошими результатами иммуносупрессивной терапии.
Лабораторные исследования для выявления таких пациентов должны включать
определение сывороточных антител к 68 кДа (hsp-70) антигену внутреннего уха.
22% пациентов с двусторонней быстро прогрессирующей SNHL и 30% пациентов с
болезнью Меньера имеют антитела к этому антигену. Анти-68 кДа (hsp-70) антитела
также встречаются у примерно 60% пациентов с двусторонним и 35% пациентов с
односторонним синдромом Меньера. В группе пациентов, у которых наблюдается
необъяснимая прогрессирующая глухота, существует приблизительно 30-процентная
вероятность того, что потеря слуха имеет иммунную этиологию. Недавние
исследования на большой группе из 279 пациентов с идиопатической двусторонней
SNHL выявили 90 (32%) положительных случаев анти-68 кДа (hsp-70) антител (среди
них 63% женщин). Антитела
к 68 кДа антигену были выявлены у пациентов, чей слух улучшился при
иммуносупрессивной терапии. Показано, что 89% пациентов с прогрессирующей
двусторонней SNHL в активной фазе имеют антитела к 68 кДа антигену, тогда как у
пациентов с неактивным заболеванием результаты всегда были отрицательными.
Среди пациентов, для которых были получены положительные результаты, у 75%
наблюдался ответ на терапию стероидами, по сравнению с 18% пациентов, у которых
результаты тестирования антител к 68 кДа антигену были отрицательными. Частота встречаемости
анти-68 кДа (hsp-70) антител при идиопатической двусторонней SNHL (IPBSNHL)
Moscicki RA et al. JAMA 272: 611-616, 1994
Корреляция анти-68kD (hsp-70) антител с активностью заболевания
В
ретроспективных исследованиях было показано, что тестирование на антитела к
антигену hsp-70 является лучшим прогностическим фактором ответа на терапию
кортикостероидами. Аутоиммунные
заболевания ЦНС рассматриваются как паранеопластические неврологические
заболевания, возникающие в результате противоопухолевого ответа иммунной
системы. К этим заболеваниям относят паранеопластический энцефаломиелит (PE),
сенсорную нейропатию (PSN), прогрессирующую дегенерацию мозжечка (PCD),
паранеопластическую миоклонию и атаксию (POMA), и синдром Стиффманна. Клинические
проявления включают потерю памяти, чувствительности, дисфункцию мозгового
ствола, мозжечковую, моторную или вегетативную дисфункцию (PE или PSN);
непроизвольные судорожные движения глаза, миоклонию и атаксию (POMA). Надежная
диагностика таких состояний - достаточно трудная задача. В большинстве случаев,
к сожалению, опухоль, являющаяся причиной развития паранеопластического
синдрома, не выявляется к тому моменту, когда у пациента наблюдаются
неврологические симптомы. Паранеопластические расстройства характеризуются
присутствием нейрональных аутоантител в сыворотке пациентов. Выявление таких
антител полезно для клинициста, т.к. подтверждает присутствие основной опухоли.
Паранеопластические нейрологические заболевания могут развиться при мелкоклеточном
раке легкого, нейробластоме, раке молочной железы, яичников и раке яичка. При
паранеопластическом синдроме выявляются следующие аутоантитела: 1. анти-Hu -
антитела к ядру нейрона I типа (anti-neuronal nuclear antibody, ANNA-1),
ассоциированы с мелкоклеточным раком легкого, приводят к развитию PE. 2. анти-Yo -
антитела к клеткам Пуркинье (PCA-1), ассоциированы с раком яичников или раком
молочной железы, приводят к развитию PCD. 3. анти-Ri - антитела к ядру нейрона II
типа (ANNA-2), ассоциированы с нейробластомой (детей) и раком фаллопиевой трубы
или молочной железы (взрослые), приводит к развитию POMA. Присутствие
таких антител подтверждает клинический диагноз паранеопластического синдрома и
ведет к целенаправленному поиску лежащей в его основе опухоли. Эти
маркеры помогают провести дифференциальную диагностику между истинным
паранеопластическим синдромом и другими воспалительными заболеваниями нервной
системы, схожими с паранеопластическим синдромом. Вестерн-иммуноблоттинг
- это чувствительный метод, который дает возможность проводить одновременно
скрининг и подтверждающее тестирование для выявления аутоантител к различным
нейрональным антигенам, присутствующим в ядрах или в цитоплазме клеток.
Анти-Hu и анти-Ri реакции можно легко наблюдать в областях 35-40 кДа и 55 кДа,
соответственно.Анатомия миелина в строении нерва
Функции
Как работают импульсы
 В спокойном состоянии внутрь нейрона попадают только ионы калия, а ионы натрия остаются снаружи. В момент возбуждения они начинаются меняться местами. Аксон положительно заряжается изнутри. Затем натрий перестает поступать через мембрану, а отток калия не прекращается.
В спокойном состоянии внутрь нейрона попадают только ионы калия, а ионы натрия остаются снаружи. В момент возбуждения они начинаются меняться местами. Аксон положительно заряжается изнутри. Затем натрий перестает поступать через мембрану, а отток калия не прекращается.Состав
Роль липидов в строении оболочки
Роль белков
Дефекты миелинизации
 Разрушение миелинового слоя нервной системы – очень серьезная патология, из-за которой происходит нарушение передачи нервного импульса. Она вызывает опасные заболевания, зачастую несовместимые с жизнью. Существуют два типа факторов, влияющие на возникновение демиелинизации:
Разрушение миелинового слоя нервной системы – очень серьезная патология, из-за которой происходит нарушение передачи нервного импульса. Она вызывает опасные заболевания, зачастую несовместимые с жизнью. Существуют два типа факторов, влияющие на возникновение демиелинизации:Почему происходит разрушение
Заболевания вследствие демиелинизации
Принципы лечения дефектов оболочки
Возможности восстановления миелина
Терапия

Прогноз по заболеваниям
Оглавление
Сокращения раздела
Нейроспецифические
белки
Основной белок миелина
(MBP)
Нейронспецифическая
енолаза (NSE)
Нейротропин-3 (NT3) и
нейротропин-4/5 (NT4/5)
Нейротрофический фактор
головного мозга (BDNF)
Цилиарный
нейротрофический фактор (CNTF)
Фосфорилированный
нейрофиламент Н (pNF-H)
Пигментный фактор
эпителиального происхождения (PEDF)
Глиальный фибриллярный
кислый протеин (GFAP)
Болезнь Альцгеймера
Рецептор конечных
продуктов гликозилирования (RAGE)
Никастрин
β-амилоид (Ab40, Ab42)
Chlamydia pneumoniae
Болезнь Альцгеймера:
роль оксидативного стресса
Маркеры функционального
состояния эпифиза
Мелатонин и мелатонин
сульфат
Серотонин
Аутоиммунные
заболевания нервной системы
Диагностическая
значимость определения аутоантител к гликолипидам при периферических НП:
Антитела к
миелинасcоциированному гликопротеину (анти-МАG)
Клинические синдромы/специфические антитела
MAG SGPG
GM1
асиало-
GM1
GM2
GD1a
GD1b
GQ1b
Синдром Гийена-Барре (GBS)
+++
IgG
IgG>IgM
20-30%
(+)
+
IgM
6%
+
IgG
5%
+
IgG
2%
Варианты GBS: AMSAN и AMSAN
+++
+
+++
+
GBS с офтальмоплегией
++
IgG GBS с атаксическим синдромом
++
GBS как осложнение CMV инфекции
+ IgM
+++
IgG >90% Синдром Миллера-Фишера
Мультифокальная моторная
нейропатия (MMN)
++
IgM
20-80% (+)
+
Синдром поражения
нижнего мотонейрона
(+)
IgM 5% +
Нейропатия, ассоциированная
с анти-MAG/SGPG IgM монокло-
нальной гаммапатией +++
м-IgM
50%
Двигательная нейропатия,
ассоциированная с IgM моноклональной гаммапатией
+++
м-IgM
10%
+++
Сенсорная атаксическая нейропатия и синдром CANOMAD
+++
м-IgM +++
м-IgM Хроническая воспалительная
демиелинизирующая полинейропатия (CIDP) ++
м-IgM +
Антитела к
сульфатированному глюкуронат параглобозиду (SGPG)
Антитела к ганглиозидам
(GanglioCombi)
Антитела к ганглиозиду
М1 (анти-GM1 аутоантитела)
Антитела к ганглиозиду
GD1b (анти-GD1b аутоантитела)
Антитела к ганглиозиду
GQ1b (анти-GQ1b аутоантитела)
Антитела к интерферону
β (анти-IFNβ антитела)
Антитела к
сфингомиелину (СМ)
Антитела к ламинину β
Антикохлеарные антитела
(анти-68 kD, hsp-70)
Заболевание
пациенты
% положительных
IPBSNHL
72
58
Отосклероз
11
0
Синдром Когана
8
0
Здоровые люди
53
2
Анти-нейрональные
аутоантитела
Системная
красная волчанка (SLE) - это аутоиммунное заболевание, для которого характерно
присутствие различных циркулирующих аутоантител. У пациентов, страдающих SLE,
часто возникают психические нарушения, их диапазон очень широк. Проявления
заболевания, связанные с ЦНС, встречаютс я у большого количества пациентов с
SLE и вызывают отклонения в поведении, напоминающие шизофрению. Приблизительно
у 90% пациентов с SLE, страдающих психическими расстройствами, выявляются
циркулирующие аутоантитела к рибосомальным белкам P. Это группа аутоантител,
направленных к рибосомальным фосфобелкам P0 (38 кДа), P1 (19 кДа) и P2 (17
кДа). Повышение аутоантител к рибосомальным белкам P может предшествовать
началу психотического эпизода. Кроме того, у таких пациентов с частотой от 17
до 80% (по различным литературным данным) выявляются также аутоантитела к РНК,
направленные против 28S рРНК. Анти-рибосомальные Р аутоантитела обычно
сосуществуют с анти-РНК аутоантителами. Показана корреляция между анти-РНК
антителами и активностью заболевания. Таким образом, и анти-рибосомальные Р, и
анти-РНК аутоантитела вносят свой вклад в патогенез расстройств ЦНС при SLE.
Антитела к
рибосомальным белкам P и РНК